AAV-Referenzmaterialien: Kapside (Vigene Bioscience)
Vigene Bioscience - Qualitätskontrolle für Ihren AAV basierten Gentransfer
Volle und leere Kapside verschiedener Adeno-assoziierter Virus-Serotypen, die häufig für den Gentransfer verwendet werden

Rekombinante Adeno-assoziierte Viren (rAAV) sind ein weit verbreitetes Instrument für die Genübertragung in der Forschung und bei klinischen Anwendungen. Um die Pharmakokinetik und Wirksamkeit von rAAV vergleichen zu können, werden gut charakterisierte Referenzmaterialien für Tests und die Kalibrierung von internen Referenzmaterialien benötigt. Referenzmaterialien mit genau definiertem Vektor-Genom-Verhältnis können in qPCR-basierten Vektor-Genom-Titrationen verwendet werden.
Es ist bekannt, dass AAV auch leere Partikel produziert und das Verhältnis von vollem zu leerem Kapsid ist ein wichtiger Qualitätsfaktor. Leere Kapside als AAV-Referenzmaterialien sind gut charakterisierte leere AAV-Viruspartikel. Hochwertige als AAV-Referenzmaterialien eingesetzte leere Kapside können als Kontrollen und Standardmaterialien in Assays, einschließlich HPLC, ELISA und allen anderen relevanten Methoden, verwendet werden.
AAV-Referenzmaterialien (leere Kapside)
| Bestellnummer | Beschreibung | Serotyp |
|---|---|---|
| RS-AAV1-ET |
AAV1 reference materials (empty capsids), 2.26x10^12 VP/mL, 100 uL |
AAV1 |
| RS-AAV2-ET |
AAV2 reference materials (empty capsids), 1.27x10^12 VP/mL, 100 uL |
AAV2 |
| RS-AAV5-ET |
AAV5 reference materials (empty capsids), 1.46x10^12 VP/mL, 100 uL |
AAV5 |
| RS-AAV6-ET |
AAV6 reference materials (empty capsids), 1.79x10^12 VP/mL, 100 uL |
AAV6 |
| RS-AAV8-ET |
AAV8 reference materials (empty capsids), 1.44x10^12 VP/mL, 100 uL |
AAV8 |
| RS-AAV9-ET |
AAV9 reference materials (empty capsids), 1.76x10^12 VP/mL, 100 uL |
AAV9 |
AAV-Referenzmaterialien (gefüllte Kapside)
| Bestellnummer | Beschreibung | Serotyp |
|---|---|---|
| RS-AAV1-FL |
AAV1 reference materials (full capsids), 5.33x10^11 GC/mL, 100 uL |
AAV1 |
| RS-AAV2-FL |
AAV2 reference materials (full capsids), 1.82x10^11 GC/mL, 100 uL |
AAV2 |
| RS-AAV5-FL |
AAV5 reference materials (full capsids), 2.60x10^11 GC/mL, 100 uL |
AAV5 |
| RS-AAV6-FL |
AAV6 reference materials (full capsids), 4.10x10^11 GC/mL, 100 uL |
AAV6 |
| RS-AAV8-FL |
AAV8 reference Materials (full capsids), 7.97x10^11 GC/mL, 100 uL |
AAV8 |
| RS-AAV9-FL |
AAV9 reference materials (full capsids), 3.86x10^11 GC/mL, 100 uL |
AAV9 |
Anwendungsgebiete für Adeno-assoziierte Viruspartikel als Referenzmaterial
AAV - gefüllte Kapside
- Referenzmaterialien für qPCR-Titer-Assays
- Kontrollen/Referenzmaterialien für Charakterisierung gefüllter / leerer Kapside
- Verifizierung von hausinterne Referenzmaterialien
AAV - leere Kapside
- Standardmaterialien für ELISA- und HPLC-Tests
- Referenzmaterialien für hauseigene Standardmaterialien
- Virale Kontrollvektoren
Weitere Informationen zur AAV-Genübertragung und AAV-Referenzmaterial herunterladen
 |
 |
Jede Charge der AAV Referenz Kapside wird mit einer Vielzahl von Methoden umfassend charakterisiert
Serotyp-spezifische AAV-Referenzmaterialien werden mit einer helfervirusfreien Methode mit dreifacher transienten Transfektion hergestellt. Die vollständigen Kapside werden durch Ultrazentrifugation isoliert, gefolgt von einer chromatographischen Reinigung. Die viralen Partikel werden sowohl mit molekularen Assays als auch mit Transmissionselektronenmikroskopie (TEM) analysiert, um den viralen Vektor vollständig zu charakterisieren, einschließlich der Titersbestimmung und des Verhältnisses von Voll- zu Leerkapsiden. Das Genom in den AAV-Referenzmaterialien ist CMV-GFP.
Alle AAV-Referenzmaterialien werden auf Identität und Reinheit, virale Partikel pro Milliliter (mL), Vektorgenome pro mL sowie auf das Verhältnis voll/leer Kapside. Die Chargengrößen liegen zwischen einigen tausend Einheiten bis zu bis Zehntausenden Einheiten je nach Serotyp und Art der Kapside (voll / leer)
TEM-Analyse von AAV-Referenzmaterialien

Abb. 1. TEM-Bild (Transmissionselektronenmikroskop) von gereinigtem AAV9-Referenzmaterial. Volle Kapside erscheinen als weiße Kugeln (weißer Pfeil), während leere Kapside als Kugeln mit schwarzen Punkten in der Mitte erscheinen (schwarzer Pfeil)
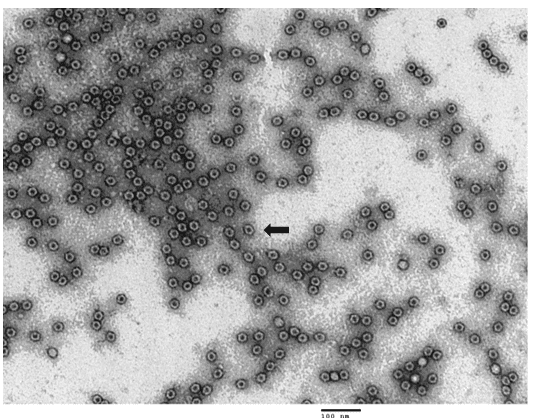
Abb.2 TEM-Aufnahme (Transmissionselektronenmikroskop) von gereinigten leeren AAV9-Partikeln. Leere Kapside erscheinen als Kugeln mit schwarzen Punkten in der Mitte (schwarzer Pfeil)
Purity of AAV Reference Materials Analyzed With Silver Staining
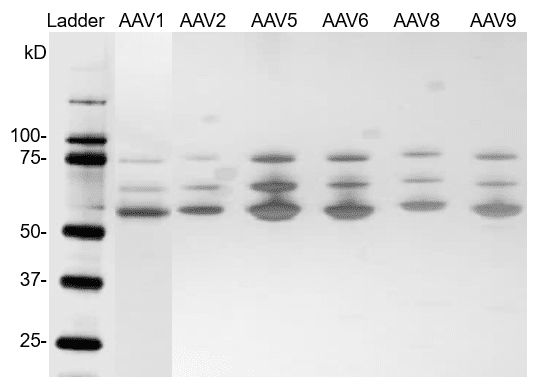
Reinheit von AAV-Referenzmaterialien mittels SDS-PAGE / Silberfärbung (gefüllte Kapside)
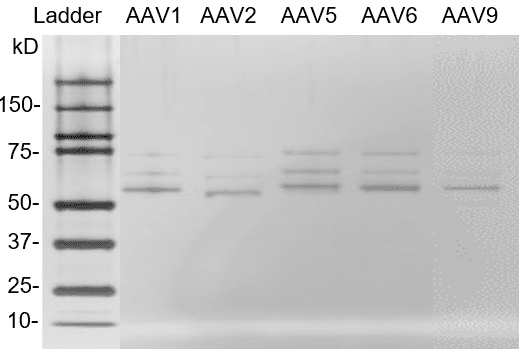
Abb. 4. Silberfärbung von AAV-Referenzmaterialien (leere Kapside). AAV-Referenzmaterialien wurden auf ein Bis-Tris-SDS-PAGE-Gel geladen. Die Proteine wurden mit Silberfärbung nachgewiesen.
Stabilität von AAV-Referenzmaterialien
Die Stabilität von AAV-Referenzmaterialien wurde mit einer separaten Stabilitätsstudie von rAAV bei 3E+12 GC/ml nachgewiesen. Die AAV-Vektoren wurden bei -80° für 2 Jahre gelagert. Der Titer des viralen Genoms und der Gesamtpartikeltiter veränderten sich durch qPCR- und ELISA-Tests nicht. Die Stabilität des Referenzmaterials (leere Kapside) wird laufend überprüft. ELISA-Tests werden nach der Lagerung bei -80°C, nach 3 Monaten, nach 6 Monaten und danach jährlich durchgeführt.
15.08.2021
Komplementsystem
Wieslab® Funktionale Assays von Svar
Langzeit-Organoid-Ku...
Afamin/Wnt3a-Komplex - jetzt mit 10 % Rabatt

Unbeschichtete ELISA...
Die kostengünstige Wahl – jetzt mit 30 % Rabatt

Mikroplastik
Referenzmaterialien von LGC Standards - mit 20 % Rabatt!
CUT&Tag-IT
Genomweite Analyse von Histonmarkierungen

