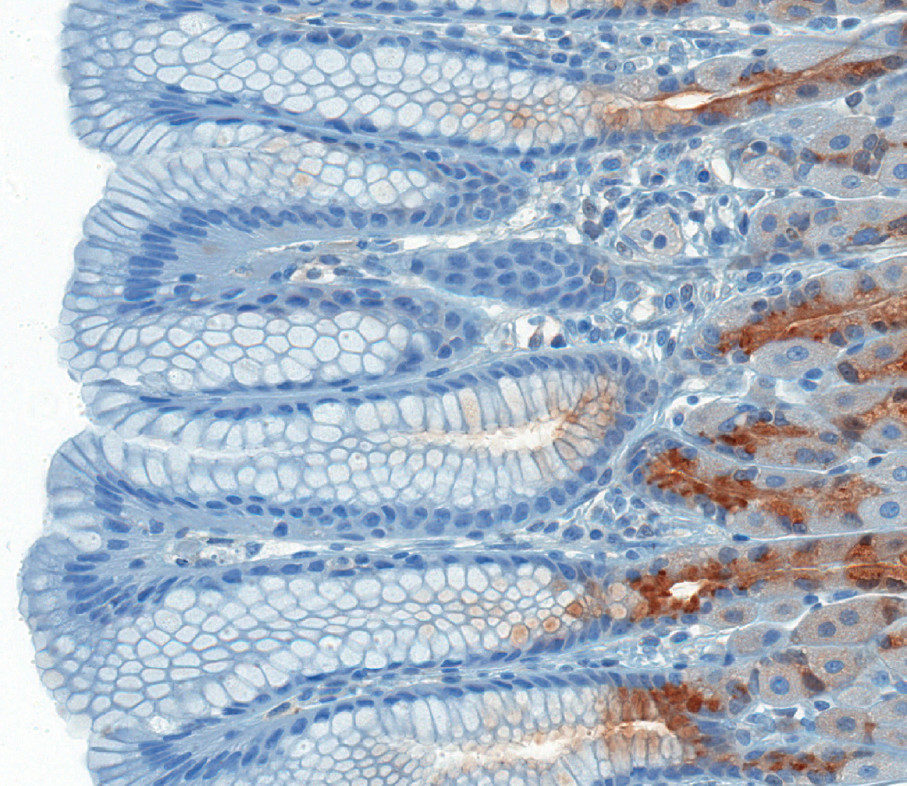
IHC-Protokoll mit Proteinase K basierter Antigengewinnung
Immunhistochemie-Protokoll für formalin-fixierte, paraffin-gebettete Gewebeschnitte
Gewebesektionierung, Deparaffinierung und Rehydrierung
-
Paraffinblöcke mit dem Mikrotom in 4-Mikron-Schnitte schneiden und auf geladene Objektträger legen (Fisher, ProbeOn, Kat. #22230900).
-
Objektträger in einem Gewebetrockenofen 45 Minuten lang bei 60°C erhitzen.
-
Waschen Sie die Objektträger 3x in Xylol für jeweils 5 Minuten bei Raumtemperatur.
-
Objektträger 3x mit 100%igem Alkohol jeweils 3 Minuten lang bei Raumtemperatur waschen.
-
Objektträger 2x mit 95%igem Alkohol jeweils 3 Minuten bei Raumtemperatur waschen.
-
Waschen der Objektträger in 80%igem Alkohol für 3 Minuten bei Raumtemperatur.
-
Objektträger 5 Minuten lang in fließendem destilliertem Wasser bei Raumtemperatur spülen.
Die folgenden Schritte sind bei Raumtemperatur durchzuführen. Die Gewebe zu keinem Zeitpunkt während des Färbevorgangs trocknen lassen.
Antigen-Entnahme
-
Objektträger in 1X TBS mit Tween (TBST) 1 Minute lang spülen.
-
Eine Arbeitslösung von Proteinase K (DAKO, Kat. #S3020) auf die Objektträger auftragen und 10 Minuten inkubieren.
- Die Objektträger 1 Minute lang mit 1X TBST spülen.
Immunfärbung mit dem AP-Vektorrot-Nachweissystem
-
Universal Protein Block (DAKO, Kat. #X0909) auf die Objektträger auftragen und 20 Minuten inkubieren.
-
Proteinblock von den Objektträgern ablaufen lassen.
-
Verdünnten Primärantikörper auf die Objektträger auftragen und 45 Minuten inkubieren.
-
Objektträger 1 Minute lang mit 1X TBST spülen und inkubieren.
-
Einen biotinylierten Sekundärantikörper auf die Objektträger (spezifisch für den Wirt des Primärantikörpers) auftragen und 30 Minuten inkubieren.
-
Die Objektträger 1 Minute lang mit 1X TBST spülen.
-
Alkalische Phosphatase Streptavidin (Vektor, Kat. #VEC-AK-5000) auf die Objektträger auftragen und 30 Minuten inkubieren.
-
Die Objektträger 1 Minute lang mit 1X TBST spülen.
-
Alkalisches Phosphatase-Chromogen-Substrat (Vektor, Kat. #VEC-AK-5000) auf die Objektträger auftragen und 30 Minuten inkubieren.
-
Die Objektträger 1 Minute lang in destilliertem Wasser waschen.
Immunfärbung mit dem HRP-DAB-Nachweissystem
-
Peroxidase-Block (3% Wasserstoffperoxid) auf die Objektträger auftragen und 5 Minuten inkubieren.
-
Objektträger 1 Minute lang mit 1X TBST spülen.
-
Universal Protein Block (DAKO, Kat. #X0909) auf die Objektträger auftragen und 20 Minuten inkubieren.
-
Proteinblock von den Objektträgern ablaufen lassen.
-
Primärantikörper auf die Objektträger auftragen und 45 Minuten inkubieren.
-
Objektträger 1 Minute lang mit 1X TBST spülen.
-
LSAB2 System-HRP LINK-Lösung (DAKO, Kat. #K0679) auf die Objektträger auftragen und 15 Minuten inkubieren.
-
Die Objektträger 1 Minute lang mit 1X TBST spülen.
-
LSAB2 System-HRP Streptavidin-HRP Lösung (DAKO, Kat. #K0679) auf die Objektträger auftragen und 10 Minuten inkubieren.
-
Die Objektträger 1 Minute lang in 1X TBST spülen.
-
Vorbereitete DAB-Substrat-Chromogen-Lösung (DAKO, Kat. #K3468) auf die Objektträger auftragen und 5 Minuten inkubieren.
-
Die Objektträger 1 Minute lang mit 1X TBST spülen.
Gegenfärbung mit Hämatoxylin
Färbung der Objektträger mit 65% Harris' Hämatoxylin für 1 Minute. Hämatoxylin färbt Nukleinsäuren (Kerne) tief blau-violett.
Dehydrierung und Deckfärbung
Diese Methode sollte nur angewendet werden, wenn das verwendete Chromogensubstrat alkoholunlöslich ist (z.B. Vektorrot oder DAB).
-
Waschen Sie die Objektträger in 2 Wechseln mit 80% Alkohol jeweils 1 Minute lang.
-
Waschen Sie die Objektträger in 2 Wechseln mit jeweils 95% Alkohol für jeweils 1 Minute.
-
Waschen der Objektträger in 3 Wechseln mit jeweils 100% Alkohol für jeweils 1 Minute.
-
Waschen der Objektträger nach 3 xylenen Wechseln für jeweils 1 Minute.
-
Deckgläser mit einem Tropfen eines permanenten Rahmungsmediums auftragen.