Kalte und heiße Tumoren
Reagenzien für die Krebsforschung von MedChem Express
 Die Untersuchung der Tumor-Mikroumgebung (TME) ist ein vielversprechender Bereich für die Entwicklung und Verbesserung von Krebstherapien. MedChem Express unterstützt Ihre Forschung mit hochwertigen Reagenzien für die Krebsforschung und Wirkstoffentwicklung.
Die Untersuchung der Tumor-Mikroumgebung (TME) ist ein vielversprechender Bereich für die Entwicklung und Verbesserung von Krebstherapien. MedChem Express unterstützt Ihre Forschung mit hochwertigen Reagenzien für die Krebsforschung und Wirkstoffentwicklung.
Mit dem Aufkommen der Krebsimmuntherapie und der Checkpoint-Inhibitoren wurden erhebliche Fortschritte bei der gezielten Manipulation der Autoimmunreaktion des Wirts als therapeutische Maßnahme zur Krebsbekämpfung erzielt, was das Feld der onkologischen Immunität und der Krebsbehandlung verändert hat. Auf Grundlage der immunen Mikroumgebung des Tumors (TME) wurde eine inoffizielle Klassifizierung von Tumoren in "kalte Tumoren" und "heiße Tumoren" entwickelt. Der heiße Tumor kann eine robuste Immunantwort hervorrufen, die es den Immunzellen ermöglicht, die Tumorzellen anzugreifen[1]. Wie ein kalter Tumor in einen heißen Tumor umgewandelt werden kann, ist ein heißes Thema der Tumorimmuntherapie.
Was sind kalte und heiße Tumoren?
Kalter Tumor: Ein kalter Tumor, auch als immundefizienter Tumor bezeichnet, zeichnet sich durch eine geringe Anzahl von CD8+ T-Zellen in der Tumormikroumgebung (TME) aus. Aufgrund der geringen Mutationslast, der Fähigkeit zur Antigenpräsentation und der PD-L1-Expression sprechen kalte Tumoren kaum auf Immun-Checkpoint-Inhibitoren (ICI) an [2].
Heißer Tumor: Forscher bezeichnen immuninflammatorische Tumoren oft als "heiße" Tumoren. Häufig gehen sie mit einer hohen T-Zell-Infiltration, PD-L1-Expression und Tumormutationslast (TMB) einher und können auf eine ICI-Therapie (Immun-Checkpoint-Inhibitor) ansprechen [3].
Wie wird aus einem kalten Tumor ein heißer Tumor?
Der Mangel an T-Zellen bei kalten Tumoren kann folgende Gründe haben: ①Mangel an Tumorantigenen, ②Mangel an APCs (Antigen-präsentierenden Zellen), ③fehlende T-Zell-Primierung/Aktivierung, ④beeinträchtigtes Trafficking von T-Zellen zur Tumormasse [5]. Entsprechend den oben genannten Faktoren werden die entsprechenden Behandlungsstrategien zur Umwandlung kalter in heiße Tumoren den Patienten zugute kommen [6,7], zum Beispiel NK-Zelltherapie, Strahlentherapie, Chemotherapie, onkolytische Virustherapie, Impfung, Zytokintherapie usw.

Figure: Strategien zur Behandlung kalter Tumore [5]
MedChem Express — Master of Bioactive Molecules
MCE bietet mehr als 20.000 Produkte und Reagenzien für die Krebsforschung an, darunter auch TME-bezogene Produkte.
| Produktname | Klassifizierung |
|---|---|
| BIO8898 | BIO8898 ist ein wirksamer CD40-CD154-Inhibitor. |
| Mitazalimab | Mitazalimab ist ein potenter FcγR-abhängiger CD40-Agonist. |
| TGFβ1-IN-1 | TGFβ1-IN-1 ist ein potenter, oral wirksamer TGF-β1-Inhibitor. |
| SRI-011381 | SRI-011381 Hydrochlorid ist ein oral wirksamer TGF-β-Signalagonist. |
| PD-1-IN-18 | PD-1-IN-18 ist ein Inhibitor des PD1-Signalweges. |
| CL845 | CL845 ist ein Analogon des STING-Agonisten CL656 (HY-112878). |
| TGF beta 1/TGFB1 protein | Das Protein TGF beta 1/TGFB1 hemmt den Zellzyklus in der G1-Phase. |
| PD-1 protein | Das PD-1-Protein unterdrückt aktivierende Signale des T-Zell-Rezeptors. |
| TMEM173 protein | Das Protein TMEM173 erleichtert die Signalübertragung des angeborenen Immunsystems. |
Referenzen:
[1] Qianqian Duan et al.,Turning Cold into Hot: Firing up the Tumor Microenvironment. Trends in Cancer, 2020, 00467 No. of Pages 14.
[2] Wculek SK, Cueto FJ, Mujal AM, et al. Dendritic cells in cancer immunology and immunotherapy. Nat Rev Immunol. 2020;20:7-24.
[3] Wei C, Ma Y, Wang F, et al. Igniting Hope for Tumor Immunotherapy: Promoting the "Hot and Cold" Tumor Transition. Clin Med Insights Oncol. 2022 Sep 15;16:11795549221120708.
[4] Appleton E, Hassan J, Chan Wah Hak C, et al. Kickstarting Immunity in Cold Tumours: Localised Tumour Therapy Combinations With Immune Checkpoint Blockade. Front Immunol. 2021 Oct 18;12:754436.
[5] Bonaventura P, Shekarian T, Alcazer V, et al. Cold Tumors: A Therapeutic Challenge for Immunotherapy. Front Immunol. 2019 Feb 8;10:168.
[6] Tumeh PC, Harview CL, Yearley JH, et al. PD-1 blockade induces responses by inhibiting adaptive immune resistance. Nature. 2014;515(7528):568–571.
[7] Mi Y, Guo N, Luan J, et al. The emerging role of myeloid-derived suppressor cells in the glioma immune suppressive microenvironment. Front Immunol. 2020;11:737.
03.08.2023
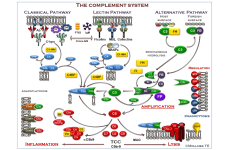
Komplementsystem
Wieslab® Funktionale Assays von Svar
Langzeit-Organoid-Ku...
Afamin/Wnt3a-Komplex

Unbeschichtete ELISA...
Die kostengünstige Wahl

Mikroplastik
Referenzmaterialien von LGC Standards
CUT&Tag-IT
Genomweite Analyse von Histonmarkierungen

